多くの創薬標的受容体(GPCR)を耐熱化する共通の方法を発見ーGPCRを標的とした創薬研究に大きく貢献ー
Research Topics / 研究トピックス
京都大学エネルギー理工学研究所の木下正弘教授は、千葉大学大学院理学研究院の村田武士教授、安田賢司特任助教らと協力して、先に開発した統計熱力学に基づく理論的予測法(エントロピー基盤法注1))を用いることにより、重要な創薬標的ファミリーであるGタンパク質共役型受容体(GPCR) を耐熱化することができる共通のアミノ酸置換箇所を発見することに成功しました。そして、関西医科大学の清水(小林)拓也教授、寿野良二講師、京都大学の岩田想教授らとの共同研究により、ムスカリンM2受容体やプロスタグランジンEP4受容体に対する耐熱化変異体(耐熱化置換体)を同定し、X線結晶構造解析注2)を用いて両受容体の立体構造の解明に成功しました。これらの耐熱化変異体では、アゴニスト注3)やアンタゴニスト注4)に対する結合親和性が変化していました。このことから、本耐熱化変異体を用いることにより立体構造解析が可能となるばかりでなく、阻害剤等のスクリーニングが容易となり、GPCRを標的とした創薬研究に大きく貢献できると期待されます。
エントロピー基盤法の論文は、2017年6月23日に米国科学雑誌「The Journal of Physical Chemistry B」に公開され、本耐熱化変異体の構造解析論文(2報)は、2018年11月12日および12月3日に米国科学雑誌「Nature Chemical Biology」に公開されました。
研究の背景と経緯
本研究では、アデノシンA2a受容体(A2aR)、M2ムスカリン受容体(M2R)、プロスタグランジンEP4受容体(EP4R)を含む8種類のヒトGPCRにエントロピー基盤法を適用し、それぞれの耐熱化変異体を予測しました。その結果、Ballesteros-Weinstein(BW)番号注5)が3.39に位置するアミノ酸残基が「ホットスポット」であり、それのアルギニンまたはリジンへの置換により耐熱化すると予測されました(図2)。そこで、A2aR、M2R、EP4Rについて実際に置換を導入し、変性温度を測定したところ、A2aRでは9℃、M2Rでは5℃、EP4Rでは6.5℃の熱変性温度の上昇が観測されました。また、これらの耐熱化変異体はアゴニスト注3)に対する結合親和性が低下する一方で、特定のアンタゴニスト注4)(阻害剤)に対する結合親和性は向上していました。これらの変異体を用いて化合物スクリーニングを行うことにより、特定の阻害剤の選別が容易になると期待されます。さらに、M2R変異体では、アンタゴニスト結合型の結晶構造の分解能が3Åから2.3Åへ向上し、新規の選択的アンタゴニスト結合型の結晶構造解析に成功しました(図3)。EP4R変異体に関してもX線回折分解能が6Åから3.4Åへ向上し、新規の結晶構造の解明に成功しました(図4)。
研究の内容
人の体の中には約800種類ものGタンパク質共役型受容体(GPCR)が存在し、生体膜内外の情報伝達に大切な役割を果たしています。このためGPCRは重要な創薬標的ファミリーであり、現在市販されている薬の約30%以上はGPCRを標的としていることが知られています。GPCRを安定かつ大量に調製できるようになれば、その機能の解明や薬のスクリーニング、X線結晶構造解析等による立体構造決定が容易になります。しかし、GPCRは一般に熱安定性が低いため取り扱いが難しく、大量調製が困難でした。私たちは最近、GPCRを含む膜タンパク質を耐熱化させるアミノ酸置換を経験則に頼らずに純理論的に予測する方法(エントロピー基盤法注1))を開発しました(国内特許登録済:第6359656号、国際特許出願中:WO2015/1991621A1) (図1)。本研究では、複数のGPCRに対してエントロピー基盤法による耐熱化変異体の予測を行うことにより、多くのGPCRの耐熱化に繋がる共通のアミノ酸置換箇所すなわち「ホットスポット」を発見しました。
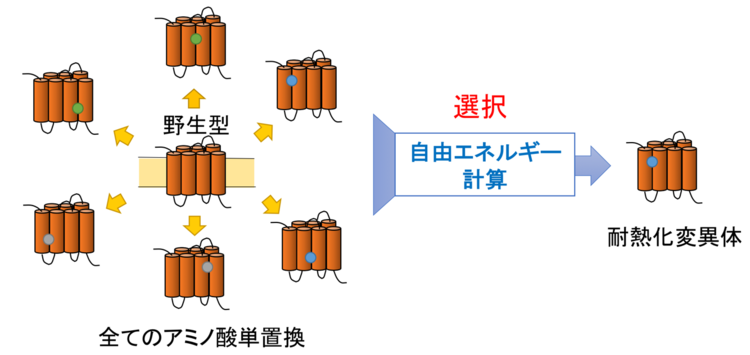
図1:エントロピー基盤法の概念図
GPCRの可能なあらゆるアミノ酸単置換を施した変異体を計算機上で発生させる。それらのアミノ酸置換に伴う自由エネルギー変化を計算し、変化量が十分大きな負の値になる置換が耐熱化をもたらすと予測する。単置換のみならず、多重置換を吟味することもできる。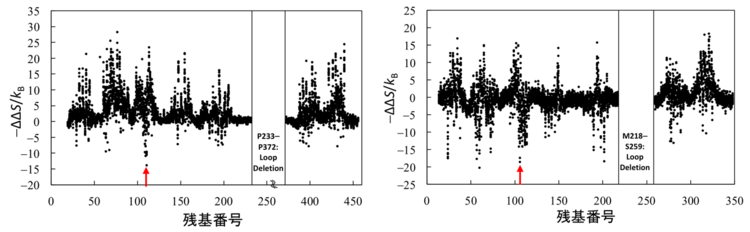
図2 エントロピー基盤法による耐熱化変異体予測の計算結果
左図がM2ムスカリン受容体に対する計算結果、右図がプロスタグランジンEP4受容体に対する計算結果である。ホットスポットであるBW番号3.39のアミノ酸残基を赤矢印で示す。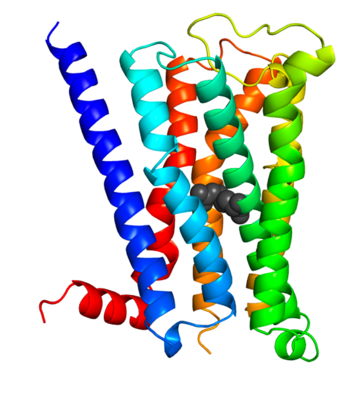
図3 M2ムスカリン受容体の耐熱化変異体の結晶構造
M2ムスカリン受容体の結晶構造のリボン図。アミノ酸置換により挿入したBW番号3.39の位置のアルギニン残基を黒色の球で表示している。
図4 プロスタグランジンEP4受容体の耐熱化変異体の結晶構造
プロスタグランジンEP4受容体の結晶構造のリボン図。アミノ酸置換により挿入したBW番号3.39の位置のアルギニン残基を黒色の球で表示している。
今後の展開
本研究により、複数のGPCRを耐熱化できる共通のアミノ酸置換箇所の発見に成功しました。このBW番号3.39のアミノ酸残基は多くのClass AのGPCRにおいて保存されており、これらのGPCRに関しても同様に耐熱化できる可能性が期待されます。本研究で発見されたアミノ酸置換により、今まで大量調製が難しかった多くの創薬標的のGPCRを耐熱化させ、大量生産することが可能になります。ただし、ホットスポット以外のアミノ酸残基を置換した方がより大きな安定化に繋がる場合や、ホットスポットの置換では安定化が得られない場合も見つかっています。いずれにせよ、アゴニスト注3)やアンタゴニスト注4)に対する結合親和性が変化する耐熱化置換箇所を数多く発見することができています。これらの性質の異なる耐熱化変異体を活用することにより、薬剤探索や機能解析・構造解析が飛躍的に進展すると期待できます。そしてこれらの構造機能情報は多くの波及効果をもたらし、関連する生命機能や疾病原因の理解から医薬品開発までの我が国のライフサイエンスの推進に大きく貢献できると考えています。
用語解説
注1)エントロピー基盤法
膜タンパク質を耐熱化させるアミノ酸置換を理論的に予測する方法。生体膜を形成するリン脂質の炭化水素鎖の並進配置エントロピーに初めて着目した点に特徴があり、可能なあらゆるアミノ酸単置換の中から耐熱化の可能性の高い候補を短時間で予測することができる。単置換のみならず、多重置換を吟味することもできる。
注2)X線結晶構造解析
解析対象のタンパク質を結晶化し、X線照射によって得られる回折データから、タンパク質の原子レベルでの立体構造を決定する手法。
注3)アゴニスト(作動薬)
受容体に結合し、神経伝達物質やホルモンなどの生体内物質(リガンド)と同様の機能を示す物質のこと。
注4)アンタゴニスト(拮抗剤)
受容体には結合するが、受容体の作用自体は起こさない物質で、本来結合すべき生体内物質が受容体に結合することを阻害する。
注5)Ballesteros-Weinstein(BW)番号
GPCR中のアミノ酸残基の位置を指定する番号。X番目のヘリックスに対して、それぞれGPCRの間で最も保存されている残基をX.50と命名する。そのヘリックス上の他のすべての残基は、この保存された位置を基準として番号付けされる。
詳しい研究内容について
Title; Structural Insights into the Subtype Selective Antagonist Binding to the M2 Muscarinic Receptor
DOI: 10.1038/s41589-018-0152-y
Title; Ligand Binding to Human Prostaglandin E Receptor EP4 at the Lipid-Bilayer Interface
DOI: 10.1038/s41589-018-0131-3
京都大学ホームページ
http://www.kyoto-u.ac.jp/ja/research/research_results/2018/181203_2.html